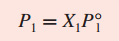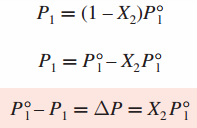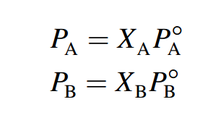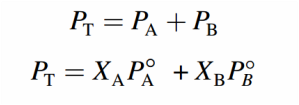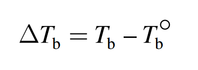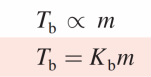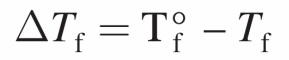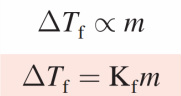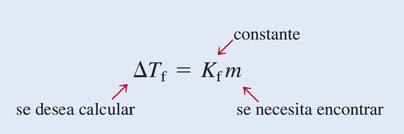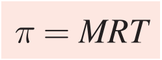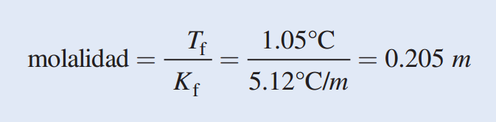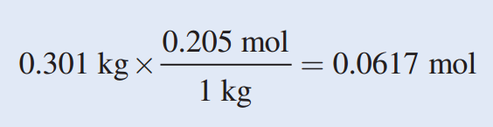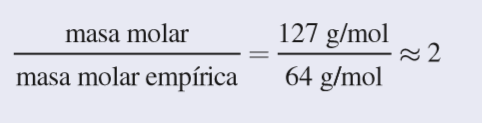Propiedades coligativas de las disoluciones de no electrólitos
Las propiedades coligativas(o propiedades colectivas) son propiedades que dependen sólo del número de partículas de soluto en la disolución y no de la naturaleza de las partículas del soluto. Todas estas propiedades tienen un mismo origen, todas dependen del número de partículas de soluto presentes, independientemente de que sean átomos, iones o moléculas.
Las propiedades coligativas son la disminución de la presión de vapor, la elevación del punto de ebullición, la disminución del punto de congelación y la presión osmótica. Para el estudio de las propiedades coligativas de disoluciones de no electrólitos es importante recordar que se está hablando de disoluciones relativamente diluidas, es decir, disoluciones cuyas concentraciones son ≤0.2 M.
Disminución de la presión de vapor
Si un soluto es no volátil(es decir, no tiene una presión de vapor que se pueda medir), la presión de vapor de sus disoluciones siempre es menor que la del disolvente puro. Así, la relación entre la presión de vapor de la disolución y la presión de vapor del disolvente puro depende de la concentración del soluto en la disolución.
Esta relación se expresa por la ley de Raoult. que establece que la presión parcial de un disolvente en una disolución, P1, está dada por la presión de vapor del disolvente puro, P°1 , multiplicada por la fracción molar del disolvente en la disolución, X1:
Las propiedades coligativas son la disminución de la presión de vapor, la elevación del punto de ebullición, la disminución del punto de congelación y la presión osmótica. Para el estudio de las propiedades coligativas de disoluciones de no electrólitos es importante recordar que se está hablando de disoluciones relativamente diluidas, es decir, disoluciones cuyas concentraciones son ≤0.2 M.
Disminución de la presión de vapor
Si un soluto es no volátil(es decir, no tiene una presión de vapor que se pueda medir), la presión de vapor de sus disoluciones siempre es menor que la del disolvente puro. Así, la relación entre la presión de vapor de la disolución y la presión de vapor del disolvente puro depende de la concentración del soluto en la disolución.
Esta relación se expresa por la ley de Raoult. que establece que la presión parcial de un disolvente en una disolución, P1, está dada por la presión de vapor del disolvente puro, P°1 , multiplicada por la fracción molar del disolvente en la disolución, X1:
En una disolución que contenga sólo un soluto, X1= 1 – X2, donde X2 es la fracción molar del soluto. Por tanto, la ecuación se puede reescribir como:
Observamos que la disminución de la presión de vapor, ∆P, es directamente proporcional a la concentración del soluto (medida en fracción molar).
¿Por qué la presión de vapor de una disolución es menor que la del disolvente puro?
Como se mencionó en molalidades, una fuerza motriz de los procesos físicos y químicos es el incremento en el desorden; a mayor desorden más favorable el proceso. La evaporación aumenta el desorden de un sistema porque las moléculas en el vapor no están muy cercanas y por tanto tienen menos orden que las de un líquido. Como en una disolución hay más desorden que en un disolvente puro, la diferencia en el desorden entre una disolución y su vapor es menor que la que hay entre un disolvente puro y su vapor. Así, las moléculas del disolvente tienen menor tendencia a abandonar la disolución que a abandonar el disolvente puro, para convertirse en vapor, y la presión de vapor de una disolución es menor que la del disolvente.
Si ambos componentes de una disolución son volátiles (es decir, tienen presiones de vapor que se pueden medir), la presión de vapor de la disolución es la suma de las presiones parciales individuales. La ley de Raoult también se cumple en este caso:
¿Por qué la presión de vapor de una disolución es menor que la del disolvente puro?
Como se mencionó en molalidades, una fuerza motriz de los procesos físicos y químicos es el incremento en el desorden; a mayor desorden más favorable el proceso. La evaporación aumenta el desorden de un sistema porque las moléculas en el vapor no están muy cercanas y por tanto tienen menos orden que las de un líquido. Como en una disolución hay más desorden que en un disolvente puro, la diferencia en el desorden entre una disolución y su vapor es menor que la que hay entre un disolvente puro y su vapor. Así, las moléculas del disolvente tienen menor tendencia a abandonar la disolución que a abandonar el disolvente puro, para convertirse en vapor, y la presión de vapor de una disolución es menor que la del disolvente.
Si ambos componentes de una disolución son volátiles (es decir, tienen presiones de vapor que se pueden medir), la presión de vapor de la disolución es la suma de las presiones parciales individuales. La ley de Raoult también se cumple en este caso:
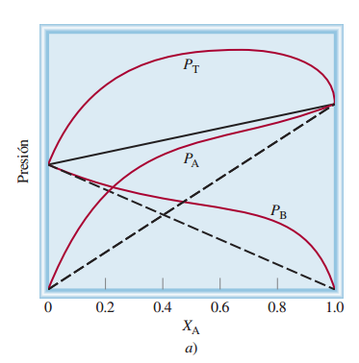
donde PA y PB son las presiones parciales de los componentes A y B de la disolución; P°A y P°B son las presiones de vapor de las sustancias puras y XA y XB son sus fracciones molares. La presión total está dada por la ley de Dalton de las presiones parciales (vea la sección 5.6):
La disolución benceno-tolueno constituye uno de los pocos ejemplos de una disolución ideal, que es cualquier disolución que obedece la ley de Raoult. Una característica de una disolución ideal es que el calor de disolución, ∆Hdisol, es cero.
La mayor parte de las disoluciones no se comporta de manera ideal en este aspecto. Se consideran los siguientes dos casos, designando dos sustancias volátiles como A y B:
Caso 1: Si las fuerzas intermoleculares entre las moléculas A y B son más débiles que las fuerzas entre las moléculas de A y las fuerzas entre las moléculas de B, entonces estas moléculas tienen mayor tendencia a abandonar la disolución que en el caso de una disolución ideal.
Como consecuencia, la presión de vapor de la disolución es mayor que la suma de las presiones de vapor predicha por la ley de Raoult para la misma concentración. Este comportamiento da lugar a una desviación positiva.
En este caso, el calor de disolución es positivo (es decir, el proceso de mezclado es endotérmico).
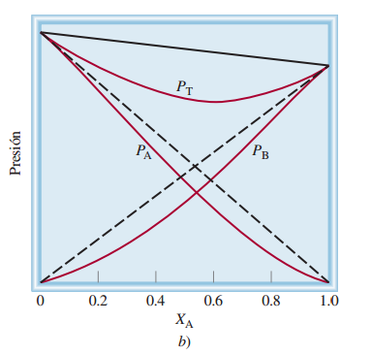
Caso 2: Si las moléculas de A atraen a las moléculas de B con más fuerza que a las de su misma clase, la presión de vapor de la disolución es menor que la suma de las presiones parciales predicha por la ley de Raoult. Esto representa una desviación negativa.
En este caso, el calor de disolución es negativo (es decir, el proceso de mezclado es exotérmico).
La mayor parte de las disoluciones no se comporta de manera ideal en este aspecto. Se consideran los siguientes dos casos, designando dos sustancias volátiles como A y B:
Caso 1: Si las fuerzas intermoleculares entre las moléculas A y B son más débiles que las fuerzas entre las moléculas de A y las fuerzas entre las moléculas de B, entonces estas moléculas tienen mayor tendencia a abandonar la disolución que en el caso de una disolución ideal.
Como consecuencia, la presión de vapor de la disolución es mayor que la suma de las presiones de vapor predicha por la ley de Raoult para la misma concentración. Este comportamiento da lugar a una desviación positiva.
En este caso, el calor de disolución es positivo (es decir, el proceso de mezclado es endotérmico).
Caso 2: Si las moléculas de A atraen a las moléculas de B con más fuerza que a las de su misma clase, la presión de vapor de la disolución es menor que la suma de las presiones parciales predicha por la ley de Raoult. Esto representa una desviación negativa.
En este caso, el calor de disolución es negativo (es decir, el proceso de mezclado es exotérmico).
Destilación fraccionada
La presión de vapor de una disolución tiene relación directa con la destilación fraccionada, procedimiento de separación de los componentes líquidos de una disolución que se basa en la diferencia en sus puntos de ebullición. La destilación fraccionada es, en cierta forma, análoga a la cristalización fraccionada. Suponga que deseamos separar un sistema binario (un sistema con dos componentes), por ejemplo, benceno-tolueno. Tanto el benceno como el tolueno son relativamente volátiles, a pesar de que sus puntos de ebullición son muy diferentes (80.1°C y 110.6°C, respectivamente). Cuando hervimos una disolución que contiene estas dos sustancias, el vapor formado es algo más rico en el componente más volátil, el benceno. Si el vapor se condensa en un recipiente distinto y se hierve de nuevo el líquido, en la fase de vapor se obtendrá una mayor concentración de benceno. Si se repite este proceso muchas veces, es posible separar por completo el benceno del tolueno.
La presión de vapor de una disolución tiene relación directa con la destilación fraccionada, procedimiento de separación de los componentes líquidos de una disolución que se basa en la diferencia en sus puntos de ebullición. La destilación fraccionada es, en cierta forma, análoga a la cristalización fraccionada. Suponga que deseamos separar un sistema binario (un sistema con dos componentes), por ejemplo, benceno-tolueno. Tanto el benceno como el tolueno son relativamente volátiles, a pesar de que sus puntos de ebullición son muy diferentes (80.1°C y 110.6°C, respectivamente). Cuando hervimos una disolución que contiene estas dos sustancias, el vapor formado es algo más rico en el componente más volátil, el benceno. Si el vapor se condensa en un recipiente distinto y se hierve de nuevo el líquido, en la fase de vapor se obtendrá una mayor concentración de benceno. Si se repite este proceso muchas veces, es posible separar por completo el benceno del tolueno.
Elevación del punto de ebullición
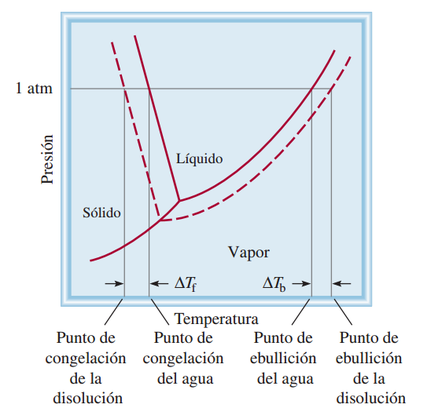
El punto de ebullición de una disolución es la temperatura a la cual su vapor de presión iguala a la presión atmosférica externa. Debido a que la presencia de un soluto no volátil disminuye la presión de vapor de una disolución, también debe afectar el punto de ebullición de la misma. En la figura se presenta el diagrama de fases del agua y los cambios que ocurren en una disolución acuosa.
El punto de ebullición de una disolución es la temperatura a la cual su vapor de presión iguala a la presión atmosférica externa. Debido a que la presencia de un soluto no volátil disminuye la presión de vapor de una disolución, también debe afectar el punto de ebullición de la misma. En la figura se presenta el diagrama de fases del agua y los cambios que ocurren en una disolución acuosa.
Debido a que a cualquier temperatura la presión de vapor de la disolución es menor que la del disolvente puro, independientemente de la temperatura, la curva líquido-vapor para la disolución siempre está por debajo de la del disolvente puro. Como consecuencia, la intersección de la curva punteada líquido-vapor y la línea horizontal que marca P = 1 atm ocurre a una temperatura mayor que el punto de ebullición normal del disolvente puro. Este análisis gráfico muestra que el punto de ebullición de la disolución es mayor que el del agua. La elevación del punto de ebullición (∆Tb) se define como el punto de ebullición de la disolución (Tb)menos el punto de ebullición del disolvente puro(T°b):
Debido a que Tb> T°b, ∆Tb es una cantidad positiva.El valor de ∆Tb es proporcional a la disminución de la presión de vapor y también es proporcional a la concentración (molalidad) de la disolución. Es decir:
donde m es la molalidad de la disolución y Kb es la constante molal de elevación del punto de ebullición. Las unidades de Kb son °C/m. Es importante entender la selección de las unidades de concentración en este caso. Se está trabajando con un sistema (la disolución) cuya temperatura no se mantiene constante, de modo que no es posible expresar la concentración en unidades de molaridad, pues ésta cambia con la temperatura.
Disminución del punto de congelación
Para una persona no científica tal vez pase inadvertido el fenómeno de la elevación del punto de ebullición, pero un observador cuidadoso, que viva en un clima frío, está familiarizado con la disminución del punto de congelación. El hielo, en las carreteras y banquetas congeladas, se derrite cuando se le espolvorean sales como NaCl o CaCl2. Este método antihielo funciona porque disminuye el punto de congelación del agua.
En la figura se observa con claridad que al disminuir la presión de vapor de la disolución, la curva sólido-líquido se desplaza hacia la izquierda. Como consecuencia, la intersección de esta línea con la línea horizontal ocurre a una temperatura menor que para el punto de congelación del agua. La disminución del punto de congelación(∆Tf) se define como el punto de congelación del disolvente puro(T°f) menos el
punto de congelación de la disolución(Tf):
Para una persona no científica tal vez pase inadvertido el fenómeno de la elevación del punto de ebullición, pero un observador cuidadoso, que viva en un clima frío, está familiarizado con la disminución del punto de congelación. El hielo, en las carreteras y banquetas congeladas, se derrite cuando se le espolvorean sales como NaCl o CaCl2. Este método antihielo funciona porque disminuye el punto de congelación del agua.
En la figura se observa con claridad que al disminuir la presión de vapor de la disolución, la curva sólido-líquido se desplaza hacia la izquierda. Como consecuencia, la intersección de esta línea con la línea horizontal ocurre a una temperatura menor que para el punto de congelación del agua. La disminución del punto de congelación(∆Tf) se define como el punto de congelación del disolvente puro(T°f) menos el
punto de congelación de la disolución(Tf):
Debido a que T°f > Tf, ∆Tf es una cantidad positiva. De nuevo, ∆Tf es proporcional a la concentración de la disolución:
donde mes la concentración del soluto en unidades de molalidad y Kf es la constante molal de la disminución del punto de congelación. Igual que para Kb, las unidades de Kf son °C/m.
Ejemplo
El etilenglicol (EG), CH2(OH)CH2(OH), es un anticongelante comúnmente utilizado en automóviles. Es soluble en agua y bastante no volátil (p. eb. 197°C). Calcule el punto de congelación de una disolución que contenga 651 g de esta sustancia en 2.505 g de agua.
¿Debe mantener esta sustancia en el radiador de su automóvil durante el verano? La masa molar del etilenglicol es de 62.01 g.
El etilenglicol (EG), CH2(OH)CH2(OH), es un anticongelante comúnmente utilizado en automóviles. Es soluble en agua y bastante no volátil (p. eb. 197°C). Calcule el punto de congelación de una disolución que contenga 651 g de esta sustancia en 2.505 g de agua.
¿Debe mantener esta sustancia en el radiador de su automóvil durante el verano? La masa molar del etilenglicol es de 62.01 g.
- Estrategia Este problema pide que se encuentre la disminución del punto de congelación de la disolución
- Solución Para encontrar el valor de la molalidad de la disolución necesitamos conocer el número de moles de EG y la masa del disolvente en kilogramos. Encontramos la masa molar del EG, convertimos la masa del disolvente en 2.505 kg, y la molalidad se calcula como sigue:
Con base en la ecuación de ∆Tf y sabindo que el Kf para el agua es 1.86 °C/m.
Debido a que el agua pura se congela a 0°C, la disolución se congelará a (0 – 7.79)°C o –7.79°C. Podemos calcular la elevación del punto de ebullición de la forma siguiente:
Debido a que la disolución hervirá a (100 +2.2)°C, o 102.2°C, sería preferible dejar el anticongelante en el radiador del automóvil en verano para evitar la ebullición de la disolución.
Ejercicio de práctica: Calcule el punto de ebullición y el punto de congelación de una disolución que contenga 478 g de etilenglicol en 3 202 g de agua.
Presión osmótica
Muchos procesos químicos y biológicos dependen de la ósmosis, el paso selectivo de moléculas del disolvente a través de una membrana porosa desde una disolución diluida hacia una de mayor concentración.
Ejercicio de práctica: Calcule el punto de ebullición y el punto de congelación de una disolución que contenga 478 g de etilenglicol en 3 202 g de agua.
Presión osmótica
Muchos procesos químicos y biológicos dependen de la ósmosis, el paso selectivo de moléculas del disolvente a través de una membrana porosa desde una disolución diluida hacia una de mayor concentración.
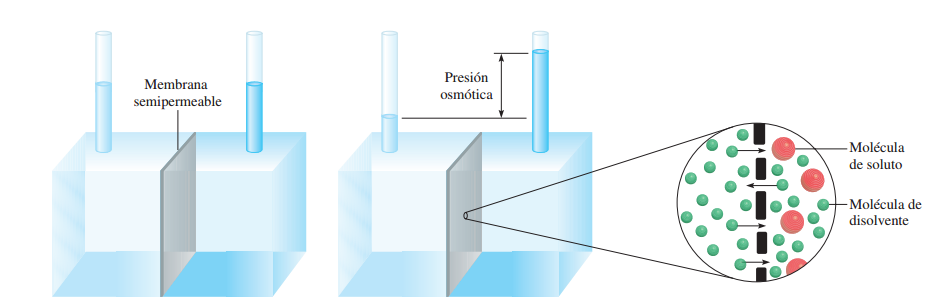
Presión osmótica.(Figura)
En la figura se ejemplifica este fenómeno. El compartimiento de la izquierda del aparato contiene el disolvente puro; el compartimiento de la derecha contiene una disolución. Los dos compartimientos están separados por medio de una membrana semipermeable, que permite el paso de moléculas del disolvente pero impide el paso de moléculas de soluto. Al principio, el nivel de agua en los dos tubos es igual(parte izq. de la figura).
Después de algún tiempo, el nivel del tubo de la derecha empieza a aumentar y continúa elevándose hasta que se alcanza el equilibrio, es decir, hasta que ya no se observa ningún cambio. La presión osmótica(π) de una disolución es la presión que se requiere para detener la ósmosis. Como se muestra en la figura (parte der), esta presión puede medirse directamente a partir de la diferencia en los niveles finales del fluido.
La presión osmótica de una disolución está dada por:
- Los niveles del disolvente puro (izquierda) y de la disolución (derecha) son iguales al principio.
- Durante la ósmosis, el nivel del lado de la disolución aumenta como resultado del flujo neto del disolvente de izquierda a derecha.
En la figura se ejemplifica este fenómeno. El compartimiento de la izquierda del aparato contiene el disolvente puro; el compartimiento de la derecha contiene una disolución. Los dos compartimientos están separados por medio de una membrana semipermeable, que permite el paso de moléculas del disolvente pero impide el paso de moléculas de soluto. Al principio, el nivel de agua en los dos tubos es igual(parte izq. de la figura).
Después de algún tiempo, el nivel del tubo de la derecha empieza a aumentar y continúa elevándose hasta que se alcanza el equilibrio, es decir, hasta que ya no se observa ningún cambio. La presión osmótica(π) de una disolución es la presión que se requiere para detener la ósmosis. Como se muestra en la figura (parte der), esta presión puede medirse directamente a partir de la diferencia en los niveles finales del fluido.
La presión osmótica de una disolución está dada por:
donde M es la molaridad de la disolución, R la constante de los gases (0.0821 L · atm/K · mol) y T la temperatura absoluta. La presión osmótica, π, se expresa en atm. Debido a que las mediciones de presión osmótica se llevan a cabo a temperatura constante, la concentración se expresa en unidades de molaridad, más convenientes que las de molalidad.
Al igual que la elevación del punto de ebullición y la disminución del punto de congelación, la presión osmótica es directamente proporcional a la concentración de la disolución. Esto es lo que se esperaría, ya que todas las propiedades coligativas dependen sólo del número de partículas de soluto disueltas en la disolución. Si dos disoluciones tienen la misma concentración, y, por tanto, la misma presión osmótica, se dice que son isotónicas. Si dos disoluciones tienen diferente presión osmótica, se dice que la disolución de mayor concentración es hipertónicay la disolución más diluida se describe como hipotónica.
Al igual que la elevación del punto de ebullición y la disminución del punto de congelación, la presión osmótica es directamente proporcional a la concentración de la disolución. Esto es lo que se esperaría, ya que todas las propiedades coligativas dependen sólo del número de partículas de soluto disueltas en la disolución. Si dos disoluciones tienen la misma concentración, y, por tanto, la misma presión osmótica, se dice que son isotónicas. Si dos disoluciones tienen diferente presión osmótica, se dice que la disolución de mayor concentración es hipertónicay la disolución más diluida se describe como hipotónica.
Empleo de las propiedades coligativas
Las propiedades coligativas de las disoluciones de no electrólitos proporcionan un medio para determinar la masa molar de un soluto.
Ejemplo
Una muestra de 7.85 g de un compuesto con la fórmula empírica C5H4 se disuelve en 301 g de benceno. El punto de congelación de la disolución es de 1.05°C por debajo del punto de congelación del benceno puro.
¿Cuál será la masa molar y la fórmula molecular de este compuesto?
Las propiedades coligativas de las disoluciones de no electrólitos proporcionan un medio para determinar la masa molar de un soluto.
Ejemplo
Una muestra de 7.85 g de un compuesto con la fórmula empírica C5H4 se disuelve en 301 g de benceno. El punto de congelación de la disolución es de 1.05°C por debajo del punto de congelación del benceno puro.
¿Cuál será la masa molar y la fórmula molecular de este compuesto?
- Estrategia La solución de este problema requiere tres pasos: en primer lugar, se calculará la molalidad de la disolución a partir de la disminución del punto de congelación. Después, a partir de la molalidad se determina el número de moles en 7.85 g de compuesto y, por tanto, su masa molar. Por último, al comparar la masa molar experimental con la masa molar empírica podremos escribir la fórmula molecular.
- Solución La secuencia de conversiones para calcular la masa molar del compuesto es
El primer paso consiste en calcular la molalidad de la disolución.
Debido que hay 0.205 moles de soluto en 1 kg de disolvente, el número de moles del soluto en 301 gramos, o 0.301 kg, de disolvente es
Por tanto, la masa molar del soluto es:
Ahora, podemos determinar la proporción
Por tanto, la fórmula molecular es de (C5H4)2 o C10H8 (naphthalene)
Ejercicio de práctica
Una disolución de 0.85 g de un compuesto orgánico en 100.0 g de benceno tiene un punto de congelación de 5.16°C. ¿Cuál es la molalidad de la disolución y la masa molar del soluto?
Ejercicio de práctica
Una disolución de 0.85 g de un compuesto orgánico en 100.0 g de benceno tiene un punto de congelación de 5.16°C. ¿Cuál es la molalidad de la disolución y la masa molar del soluto?
aca el formulario