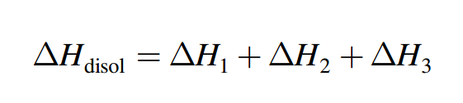Enfoque molecular del proceso de disolución
Las atracciones intermoleculares que mantienen juntas a las moléculas en líquidos y sólidos también tienen una función importante en la formación de las disoluciones. Cuando una sustancia (el soluto) se disuelve en otra (el disolvente), las partículas del soluto se dispersan en el disolvente. Las partículas de soluto ocupan posiciones que estaban ocupadas por moléculas de disolvente. La facilidad con la que una partícula de soluto reemplaza a una molécula de disolvente depende de la fuerza relativa de tres tipos de interacciones:
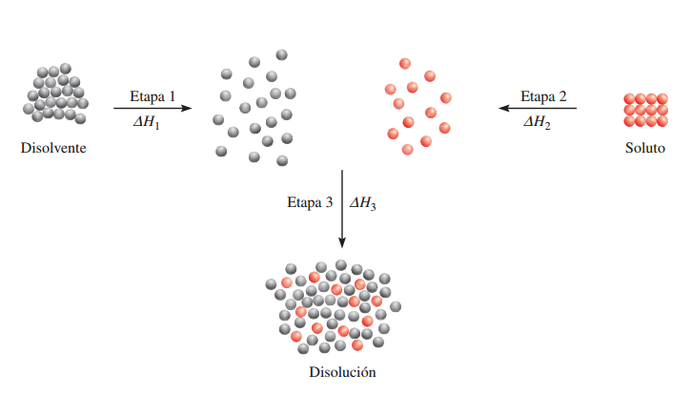
Por simplificación, entendemos que el proceso de disolución se lleva a cabo en tres etapas diferentes. La etapa 1 es la separación de las moléculas del disolvente y la etapa 2 implica la separación de las moléculas del soluto. Estas etapas requieren energía para romper las fuerzas de atracción intermoleculares; como consecuencia, son endotérmicas. En la etapa 3 las moléculas del disolvente y del soluto se mezclan. Este proceso puede ser exotérmico o endotérmico.
- interacción disolvente-disolvente
- interacción soluto-soluto
- interacción disolvente-soluto
Por simplificación, entendemos que el proceso de disolución se lleva a cabo en tres etapas diferentes. La etapa 1 es la separación de las moléculas del disolvente y la etapa 2 implica la separación de las moléculas del soluto. Estas etapas requieren energía para romper las fuerzas de atracción intermoleculares; como consecuencia, son endotérmicas. En la etapa 3 las moléculas del disolvente y del soluto se mezclan. Este proceso puede ser exotérmico o endotérmico.
El calor de disolución ∆Hdisol está dado por:
Si la atracción soluto-disolvente es mayor que la atracción disolvente-disolvente y que la atracción soluto-soluto, el proceso de disolución será favorable o exotérmico (∆Hdisol< 0).
Si la interacción soluto-disolvente es más débil que las interacciones disolvente-disolvente y soluto-soluto, el proceso de disolución será endotérmico (∆Hdisol> 0).
Resulta sorprendente el hecho de que un soluto pueda disolverse en un disolvente si la atracción entre sus propias moléculas es más fuerte que la atracción soluto-disolvente. El proceso de disolución, igual que todos los procesos físicos y químicos, está regido por dos factores. Uno es el factor energético, que determina si un proceso de disolución es exotérmico o endotérmico. El segundo factor se refiere a la tendencia hacia el desorden inherente a todos los procesos naturales. Lo mismo que las cartas de una baraja se mezclan al barajarse, cuando se mezclan las moléculas de soluto y de disolvente para formar una disolución, hay un incremento de aleatoriedad, o desorden. En estado puro, el disolvente y el soluto poseen cierto grado de orden, que se caracteriza por la disposición más o menos regular de átomos, moléculas o iones en el espacio tridimensional. Gran parte de este orden se destruye cuando el soluto se disuelve en el disolvente. Por tanto, el proceso de disolución
Si la interacción soluto-disolvente es más débil que las interacciones disolvente-disolvente y soluto-soluto, el proceso de disolución será endotérmico (∆Hdisol> 0).
Resulta sorprendente el hecho de que un soluto pueda disolverse en un disolvente si la atracción entre sus propias moléculas es más fuerte que la atracción soluto-disolvente. El proceso de disolución, igual que todos los procesos físicos y químicos, está regido por dos factores. Uno es el factor energético, que determina si un proceso de disolución es exotérmico o endotérmico. El segundo factor se refiere a la tendencia hacia el desorden inherente a todos los procesos naturales. Lo mismo que las cartas de una baraja se mezclan al barajarse, cuando se mezclan las moléculas de soluto y de disolvente para formar una disolución, hay un incremento de aleatoriedad, o desorden. En estado puro, el disolvente y el soluto poseen cierto grado de orden, que se caracteriza por la disposición más o menos regular de átomos, moléculas o iones en el espacio tridimensional. Gran parte de este orden se destruye cuando el soluto se disuelve en el disolvente. Por tanto, el proceso de disolución
Es acompañado por aumento del desorden. Este aumento es en el desorden del sistema, lo que favorece la solubilidad de una sustancia, incluso si el proceso de disolución es endotérmico. La solubilidad es una medida de la cantidad de soluto que se disolverá en cierto disolvente a una temperatura específica. El dicho “lo semejante disuelve a lo semejante” es de gran ayuda para predecir la solubilidad de una sustancia en determinado disolvente. Esta expresión significa que es probable que dos sustancias cuyas fuerzas intermoleculares son del mismo tipo y magnitud sean solubles entre sí. Por ejemplo, tanto el tetracloruro de carbono (CCl4) como el benceno (C6H6) son líquidos no polares.
Las únicas fuerzas intermoleculares presentes en estas sustancias son las fuerzas de dispersión. Cuando se mezclan estos dos líquidos, rápidamente se disuelven uno en otro, porque las fuerzas de atracción entre las moléculas de CCl4y de C6H6 son parecidas en magnitud a las fuerzas que se dan entre las moléculas de CCl4y entre las moléculas de C6H6.
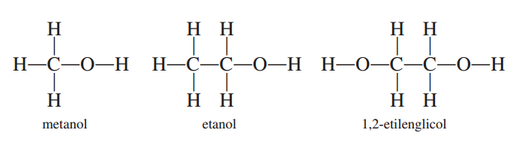
Se dice que dos líquidos son miscibles si son completamente solubles entre sí en todas proporciones. Los alcoholes, como metanol, etanol y 1,2-etilenglicol son miscibles con agua porque forman puentes de hidrógeno con las moléculas de agua:
Se dice que dos líquidos son miscibles si son completamente solubles entre sí en todas proporciones. Los alcoholes, como metanol, etanol y 1,2-etilenglicol son miscibles con agua porque forman puentes de hidrógeno con las moléculas de agua:
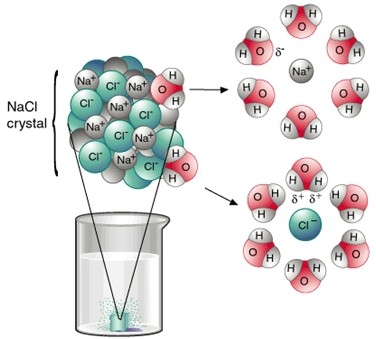
Cuando el cloruro de sodio se disuelve en agua, los iones se estabilizan en disolución por la hidratación, que implica interacciones ion-dipolo. En general, podemos predecir que los compuestos iónicos serán mucho más solubles en disolventes polares, como agua, amoniaco líquido y fluoruro de hidrógeno líquido, que en disolventes no polares, como benceno y tetracloruro de carbono. Debido a que las moléculas de los disolventes no polares carecen de un momento dipolar, no pueden solvatar a los iones Na+y Cl–. (Solvataciónes el proceso mediante el cual un ion o una molécula se rodea por moléculas del disolvente, distribuidas de una forma específica. Cuando el disolvente es agua, este proceso se llama hidratación.)
Las interacciones intermoleculares que predominan entre los iones y los compuestos no polares son las interacciones ion-dipolo inducido, que son mucho más débiles que las interacciones ion-dipolo. Como consecuencia, los compuestos iónicos por lo general son muy poco solubles en disolventes no polares.
Las interacciones intermoleculares que predominan entre los iones y los compuestos no polares son las interacciones ion-dipolo inducido, que son mucho más débiles que las interacciones ion-dipolo. Como consecuencia, los compuestos iónicos por lo general son muy poco solubles en disolventes no polares.