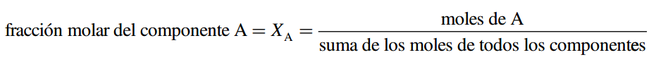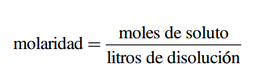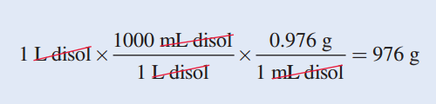Unidades de concentración
El estudio cuantitativo de una disolución requiere que se conozca su concentración, es decir, la cantidad de soluto presente en determinada cantidad de una disolución. Los químicos utilizan varias unidades de concentración diferentes; cada una de ellas tiene ciertas ventajas, así como algunas limitaciones.
Examinaremos las cuatro unidades de concentración más comunes: porcentaje en masa, fracción molar, molaridad y molalidad.
Examinaremos las cuatro unidades de concentración más comunes: porcentaje en masa, fracción molar, molaridad y molalidad.
Tipos de unidades de concentración:
- Porcentaje en masa: El porcentaje en masa(también llamado porcentaje en peso o peso porcentual) es la relación de la masa de un soluto en la masa de la disolución, multiplicado por 100%
- Fracción molar (X): El concepto de fracción molar lo introdujimos en la sección 5.6. La fracción molar de un componente de una disolución, el componente A, se representa como XA y se define como:
La fracción molar no tiene unidades, debido a que también representa una relación de dos cantidades semejantes.
- Molaridad (M): La molaridad es el número de moles de soluto en 1L de disolución, es decir:
Por tanto, las unidades de la molaridad son moles/L.
- Molalidad (m): La molalidades el número de moles de soluto disueltos en 1kg de un disolvente, es decir:
----------------------------------------------------------------------- preguntar
Por ejemplo, para preparar una disolución acuosa de sulfato de sodio (Na2SO4)
1 molal, o 1 m, es necesario disolver 1 mol (142.0 g) de la sustancia en 1 000 g (1 kg) de agua.
Dependiendo de la naturaleza de la interacción soluto-disolvente, el volumen final
de la disolución será mayor o menor que 1 000 mL. También es posible, aunque poco probable,
que el volumen final sea igual a 1 000 mL
-----------------------------------------------------------------------
Por ejemplo, para preparar una disolución acuosa de sulfato de sodio (Na2SO4)
1 molal, o 1 m, es necesario disolver 1 mol (142.0 g) de la sustancia en 1 000 g (1 kg) de agua.
Dependiendo de la naturaleza de la interacción soluto-disolvente, el volumen final
de la disolución será mayor o menor que 1 000 mL. También es posible, aunque poco probable,
que el volumen final sea igual a 1 000 mL
-----------------------------------------------------------------------
Comparación entre las unidades de concentración
La elección de una unidad de concentración depende del propósito del experimento. Por ejemplo, la fracción molar no se utiliza para expresar la concentración de las disoluciones para valoraciones o para análisis gravimétricos, pero es apropiada para el cálculo de presiones parciales de los gases y para trabajar con presiones de vapor de las disoluciones (que se analizará más adelante, en este capítulo).
La ventaja de la molaridad radica en que, por lo general, es más fácil medir el volumen de una disolución, utilizando matraces volumétricos calibrados con precisión, que pesar el disolvente, Por esta razón, en general se prefiere la molaridad sobre la molalidad. Por otra parte, la molalidad es independiente de la temperatura, ya que la concentración se expresa en número de moles de soluto y masa de disolvente. El volumen de una disolución aumenta al incrementarse la temperatura, de modo que una disolución que es 1.0 Ma 25°C podría llegar a ser 0.97 Ma 45°C debido al aumento del volumen. La dependencia de la concentración con respecto de la temperatura puede afectar de manera significativa la exactitud de un experimento. Por tanto, en algunas ocasiones es preferible utilizar molalidad en vez de molaridad.
El porcentaje en masa es semejante a la molalidad en que es independiente de la temperatura. Además, como se define en términos de relación de masa de soluto y masa de disolución, no necesitamos conocer la masa molar del soluto para calcular el porcentaje en masa.
La elección de una unidad de concentración depende del propósito del experimento. Por ejemplo, la fracción molar no se utiliza para expresar la concentración de las disoluciones para valoraciones o para análisis gravimétricos, pero es apropiada para el cálculo de presiones parciales de los gases y para trabajar con presiones de vapor de las disoluciones (que se analizará más adelante, en este capítulo).
La ventaja de la molaridad radica en que, por lo general, es más fácil medir el volumen de una disolución, utilizando matraces volumétricos calibrados con precisión, que pesar el disolvente, Por esta razón, en general se prefiere la molaridad sobre la molalidad. Por otra parte, la molalidad es independiente de la temperatura, ya que la concentración se expresa en número de moles de soluto y masa de disolvente. El volumen de una disolución aumenta al incrementarse la temperatura, de modo que una disolución que es 1.0 Ma 25°C podría llegar a ser 0.97 Ma 45°C debido al aumento del volumen. La dependencia de la concentración con respecto de la temperatura puede afectar de manera significativa la exactitud de un experimento. Por tanto, en algunas ocasiones es preferible utilizar molalidad en vez de molaridad.
El porcentaje en masa es semejante a la molalidad en que es independiente de la temperatura. Además, como se define en términos de relación de masa de soluto y masa de disolución, no necesitamos conocer la masa molar del soluto para calcular el porcentaje en masa.
Ejemplo
La densidad de una disolución acuosa de metanol (CH3OH) 2.45 Mes de 0.976 g/mL. ¿Cuál es la molalidad de la disolución? La masa molar del metanol es de 32.04 g.
La densidad de una disolución acuosa de metanol (CH3OH) 2.45 Mes de 0.976 g/mL. ¿Cuál es la molalidad de la disolución? La masa molar del metanol es de 32.04 g.
- Estrategia Para calcular la molalidad, necesitamos conocer el número de moles de metanol y la masa del disolvente en kilogramos. Suponemos que hay 1 L de disolución, así que el número de moles de metanol es de 2.45 moles.
- Solución El primer paso es calcular la masa de agua en un litro de disolución, mediante el uso de la densidad como factor de conversión. La masa total de 1 L de disolución de metanol 2.45 M.
Es debido a que esta disolución contiene 2.45 moles de metanol, la cantidad de agua (disolvente) en la disolución es
La molalidad de la disolución se puede calcular mediante la conversión de 898 g a 0.898 kg:
Ejercicio de práctica:
Calcule la molalidad de una disolución de etanol (C2H5OH) 5.86 M cuya densidad es de 0.927 g/mL.
Calcule la molalidad de una disolución de etanol (C2H5OH) 5.86 M cuya densidad es de 0.927 g/mL.
ACA UN FORMULARIO QUE RECIBA LA RESPUESTA PARA DECIR SI ES CORRECTO